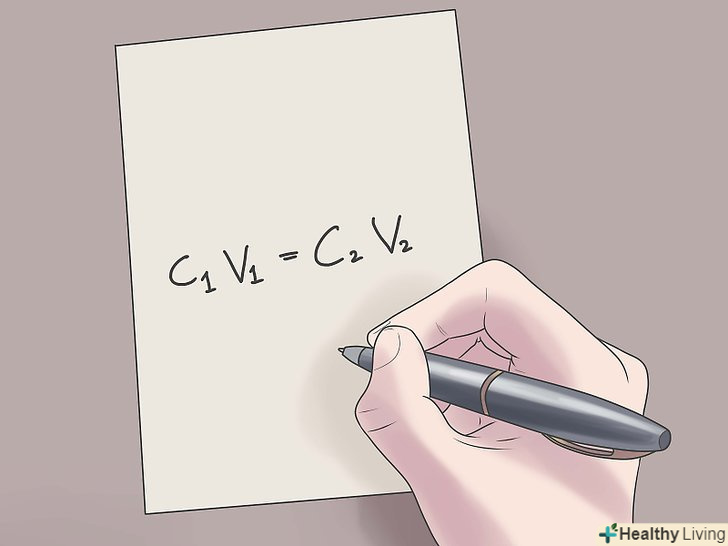В результаті розведення розчин стає менш концентрованим. Розчини розбавляють (розводять) до менших концентрацій з різних причин. Наприклад, біохіміки розбавляють концентровані розчини з метою отримання нових розчинів, які вони потім використовують у своїхекспериментах. Бармени ж нерідко розводять міцні напої більш м'якими або соками, щоб отримати коктейлі, приємні на смак. Для розрахунку ступеня розведення використовуйте формулу C1V1 = C2V2, де C1 і C2 — початкова і кінцева концентрація розчину відповідно, а V1 і V2 — початковий і кінцевий обсяг.
Кроки
Метод1 З 2:
Точний розрахунок концентрацій
Метод1 З 2:
 Визначте, що вам відомо і що ні.у хімії розведення зазвичай означає отримання невеликої кількості розчину відомої концентрації з подальшим його розведенням нейтральною рідиною (наприклад водою) і отриманням, таким чином, менш концентрованого розчину більшого обсягу. Ця операція дуже часто застосовується в хімічних лабораторіях, тому в них реагенти зберігаються для зручності в концентрованому вигляді і розбавляються при необхідності. На практиці, як правило, відома початкова концентрація, а також концентрація і обсяг розчину, який необхідно отримати; при цьому невідомий обсяг концентрованого розчину, який потрібно розбавити.
Визначте, що вам відомо і що ні.у хімії розведення зазвичай означає отримання невеликої кількості розчину відомої концентрації з подальшим його розведенням нейтральною рідиною (наприклад водою) і отриманням, таким чином, менш концентрованого розчину більшого обсягу. Ця операція дуже часто застосовується в хімічних лабораторіях, тому в них реагенти зберігаються для зручності в концентрованому вигляді і розбавляються при необхідності. На практиці, як правило, відома початкова концентрація, а також концентрація і обсяг розчину, який необхідно отримати; при цьому невідомий обсяг концентрованого розчину, який потрібно розбавити.- В іншій ситуації, наприклад при вирішенні шкільної завдання з хімії, в якості невідомої може виступати інша величина: наприклад, дані початковий обсяг і концентрація, і потрібно знайти кінцеву концентрацію підсумкового розчину при його відомому обсязі. У будь-якому випадку корисно виписати відомі і невідомі величини, перш ніж приступати до завдання.[1]
- Розглянемо приклад. Нехай нам необхідно розвести розчин концентрацією 5 M, щоб отримати розчин концентрацією 1 мМ. В даному випадку нам відома концентрація початкового розчину, а також обсяг і концентрація розчину, який необхідно отримати;не відомий обсяг вихідного розчину, який треба розвести водою.
- Пам'ятайте: в хімії М служить мірою концентрації, званої такожмолярністю, яка відповідає кількості молей речовини на 1 літр розчину.
 Підставте відомі значення у формулу c1V1 = C2V2 . у цій формулі c1 — концентрація початкового розчину, V1 — його обсяг, c2 — концентрація кінцевого розчину, і V2 — його обсяг. З отриманого рівняння ви без праці визначите шукану величину.[2]
Підставте відомі значення у формулу c1V1 = C2V2 . у цій формулі c1 — концентрація початкового розчину, V1 — його обсяг, c2 — концентрація кінцевого розчину, і V2 — його обсяг. З отриманого рівняння ви без праці визначите шукану величину.[2]- Іноді корисно поставити знак питання перед величиною, яку потрібно знайти.
- Повернемося до нашого прикладу. Підставимо в рівність відомі нам значення:
- C1V1 = C2V2
- (5 M)V1 = (1 мМ) (1 л). Концентрації мають різні одиниці виміру. Зупинимося на цьому трохи докладніше.
 Враховуйте будь-яку відмінність в одиницях виміру.оскільки розбавлення призводить до зменшення концентрації, і нерідко значного, іноді концентрації виміряні в різних одиницях. Якщо упустити це, ви можете помилитися з результатом на кілька порядків. Перед вирішенням рівняння приведіть всі значення концентрації та об'єму до однакових одиниць виміру.
Враховуйте будь-яку відмінність в одиницях виміру.оскільки розбавлення призводить до зменшення концентрації, і нерідко значного, іноді концентрації виміряні в різних одиницях. Якщо упустити це, ви можете помилитися з результатом на кілька порядків. Перед вирішенням рівняння приведіть всі значення концентрації та об'єму до однакових одиниць виміру.- У нашому випадку використовуються дві одиниці концентрації, M і мМ. Переведемо все в М:
- 1 мМ × 1 M/1.000 мМ
- = 0,001 M.
- У нашому випадку використовуються дві одиниці концентрації, M і мМ. Переведемо все в М:
 Вирішимо рівняння.коли ви привели всі величини до однакових одиниць виміру, можете вирішувати рівняння. Для його вирішення майже завжди достатньо знання простих алгебраїчних операцій.
Вирішимо рівняння.коли ви привели всі величини до однакових одиниць виміру, можете вирішувати рівняння. Для його вирішення майже завжди достатньо знання простих алгебраїчних операцій.- Для нашого прикладу: (5 M) V1 = (1 мМ) (1 л). Привівши все до однакових одиниць, вирішимо рівняння щодо V1.
- (5 M)V1 = (0,001 M) (1 л)
- V1 = (0,001 M)(1 л)/(5 M).
- V1 = 0,0002 л, або 0.2 мл.
- Для нашого прикладу: (5 M) V1 = (1 мМ) (1 л). Привівши все до однакових одиниць, вирішимо рівняння щодо V1.
 Подумайте про застосування отриманого результату на практиці.Припустимо, ви вирахували шукану величину, але все ще важко приготувати реальний розчин. Така ситуація цілком зрозуміла-мова математики і чистої науки іноді далекий від реального світу. Якщо вам вже відомі всі чотири величини, що входять в рівняння c1V1 = C2V2, поступите наступним чином:
Подумайте про застосування отриманого результату на практиці.Припустимо, ви вирахували шукану величину, але все ще важко приготувати реальний розчин. Така ситуація цілком зрозуміла-мова математики і чистої науки іноді далекий від реального світу. Якщо вам вже відомі всі чотири величини, що входять в рівняння c1V1 = C2V2, поступите наступним чином:- Виміряйте об'єм V1 розчину концентрацією C1. Потім долийте розводить рідина (воду тощо), щоб обсяг розчину став дорівнює V2. Цей новий розчин і буде володіти необхідною концентрацією (c2).
- У нашому прикладі ми спочатку відміряємо 0,2 мл вихідного розчину концентрацією 5 M. потім розводимо його водою до обсягу 1 л: 1 л — 0,0002 л = 0,9998 л, тобто додаємо до нього 999,8 мл води. Одержаний розчин буде мати необхідну нам концентрацію 1 мМ.
Метод2 З 2:
Отримання простих розчинів для практичних цілей
Метод2 З 2:
 Ознайомтеся з інформацією на упаковці.часто буває необхідно щось розвести на кухні або для інших домашніх цілей. Наприклад, приготувати апельсиновий сік з концентрату. У більшості випадків на упаковці продукту, призначеного до розведення, вказана інформація про те, як це зробити, причому нерідко з докладними інструкціями. При читанні інструкції, зверніть увагу на наступне:
Ознайомтеся з інформацією на упаковці.часто буває необхідно щось розвести на кухні або для інших домашніх цілей. Наприклад, приготувати апельсиновий сік з концентрату. У більшості випадків на упаковці продукту, призначеного до розведення, вказана інформація про те, як це зробити, причому нерідко з докладними інструкціями. При читанні інструкції, зверніть увагу на наступне:- Обсяг використовуваного продукту;
- Об'єм рідини, в якій треба розбавити продукт;
- Тип рідини (зазвичай вода);
- Особливі інструкції з розведення.
- Можливо, вине знайдете інформації про точний об'єм рідини, оскільки для пересічного споживача така інформація зайва.
 Додайте розводячу рідину в концентрований розчин.у домашніх умовах, наприклад на кухні, вам необхідно лише знати обсяг використовуваного концентрату і приблизний кінцевий обсяг. Розведіть концентрат необхідною кількістю рідини, що визначається об'ємом розбавляється концентрату. При цьому:
Додайте розводячу рідину в концентрований розчин.у домашніх умовах, наприклад на кухні, вам необхідно лише знати обсяг використовуваного концентрату і приблизний кінцевий обсяг. Розведіть концентрат необхідною кількістю рідини, що визначається об'ємом розбавляється концентрату. При цьому:-
якщо, наприклад, ви хочете розвести 1 чашку концентрату апельсинового соку до 1/4 його первісної концентрації, необхідно додати 3 чашки води. Таким чином, кінцевий розчин об'ємом 4 чашки буде містити одну чашку концентрату, тобто 1/4 загального обсягу.[3]
- Приклад складніше: якщо ви хочете розвести2/3 чашки концентрату до 1/4 його початкової концентрації, додайте 2 чашки води, оскільки 2/3 чашки — це 1/4 частина загального об'єму рідини 2х2/3 чашки.
- Переконайтеся заздалегідь, що приготовані ємності достатні, щоб вмістити весь кінцевий обсяг рідини; використовуйте велику чашку або миску.
 Як правило, обсяг порошку концентрату можна не враховувати.зазвичай додавання невеликої кількість порошку не призводить до скільки-небудь помітного зміни об'єму рідини. Іншими словами, можете засипати порошок в рідину кінцевого обсягу і розмішати.
Як правило, обсяг порошку концентрату можна не враховувати.зазвичай додавання невеликої кількість порошку не призводить до скільки-небудь помітного зміни об'єму рідини. Іншими словами, можете засипати порошок в рідину кінцевого обсягу і розмішати.
Попередження
- Дотримуйтеся інструкцій з безпеки, обумовлених виробником або правилами вашої компанії. Це особливо важливо в разі, якщо ви розбавляєте розчин будь-якої кислоти.
- При роботі з розчинами кислот вам знадобляться додаткові інструкції з розведення і правилам безпеки.