Сульфат міді-це неорганічна сполука, яка широко використовується в різних пестицидах для боротьби з шкідливими бактеріями, водоростями, рослинами, равликами і грибами.[1] він являє собою з'єднання оксиду міді з сірчаною кислотою. Сульфат міді часто використовується також для вирощування ефектних синіх кристалів при демонстраційних наукових експериментах.[2]
Увага: При проведенні нижчеописаних дослідів обов'язкова присутність дорослих
Кроки
Метод1З 3:
Приготування розчину сульфату міді
Метод1З 3:
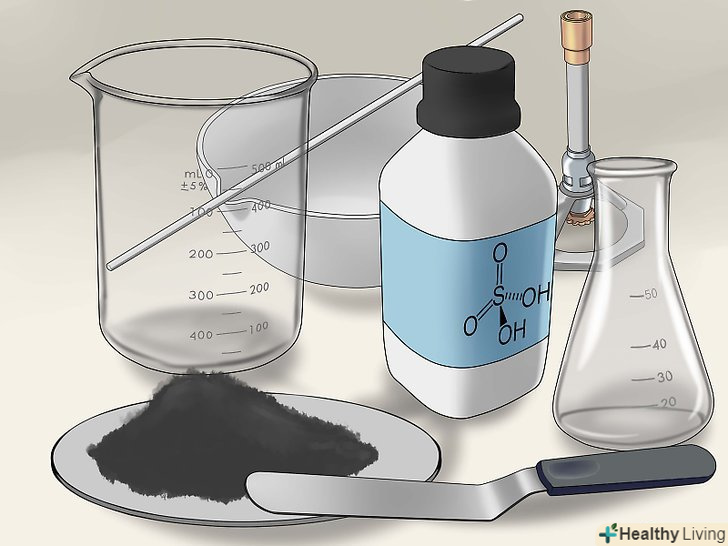
 Зберіть все необхідне.розмістіть всі матеріали та інструменти в одному місці, щоб вам не довелося перериватися під час роботи в пошуках чогось відсутнього. Вам знадобиться наступне: [3]
Зберіть все необхідне.розмістіть всі матеріали та інструменти в одному місці, щоб вам не довелося перериватися під час роботи в пошуках чогось відсутнього. Вам знадобиться наступне: [3]- Оксид міді
- Сірчана кислота
- Захисні окуляри
- Скляний хімічний стакан
- Конічна колба
- Лопаточка
- Скляна паличка для перемішування
- Чашка для випарювання
- Бунзенівський пальник
- Тринога
- Фільтрувальний папір
- Фільтрувальна воронка
 Приготуйте робоче місце.поставте скляний хімічний стакан на триногу над бунзеновской пальником. Одягніть захисні окуляри.[4]
Приготуйте робоче місце.поставте скляний хімічний стакан на триногу над бунзеновской пальником. Одягніть захисні окуляри.[4] Налийте в скляну склянку сірчану кислоту.розігрійте її, не доводячи до кипіння.[5]
Налийте в скляну склянку сірчану кислоту.розігрійте її, не доводячи до кипіння.[5] Додайте в кислоту трохи оксиду міді.використовуйте для цього лопатку, щоб не обпектися.[6]
Додайте в кислоту трохи оксиду міді.використовуйте для цього лопатку, щоб не обпектися.[6] Злегка розмішайте рідину скляною паличкою.не слід перемішувати кислоту занадто сильно, інакше вона може бризнути вам на шкіру. Перемішуйте її протягом приблизно 30 секунд кожен раз після додавання чергової порції оксиду міді.[7]
Злегка розмішайте рідину скляною паличкою.не слід перемішувати кислоту занадто сильно, інакше вона може бризнути вам на шкіру. Перемішуйте її протягом приблизно 30 секунд кожен раз після додавання чергової порції оксиду міді.[7] Продовжуйте підігрівати розчин після того, як додасте в нього весь оксид міді.це необхідно для протікання хімічної реакції. Може знадобитися від 1 до 2 хвилин. При цьому розчин помутніє і в ньому з'явиться чорний порошок.[8]
Продовжуйте підігрівати розчин після того, як додасте в нього весь оксид міді.це необхідно для протікання хімічної реакції. Може знадобитися від 1 до 2 хвилин. При цьому розчин помутніє і в ньому з'явиться чорний порошок.[8] Вимкніть пальник.за допомогою лакмусового паперу можна переконатися в тому, що в розчині не залишилося кислоти. Якщо кислота залишилася, після фільтрування розчину з'являться її пари.[9]
Вимкніть пальник.за допомогою лакмусового паперу можна переконатися в тому, що в розчині не залишилося кислоти. Якщо кислота залишилася, після фільтрування розчину з'являться її пари.[9] Відставте склянку з розчином в сторону.Дайте розчину охолонути, поки ви готуєтеся до процесу фільтрування.[10]
Відставте склянку з розчином в сторону.Дайте розчину охолонути, поки ви готуєтеся до процесу фільтрування.[10]
Метод2 З 3:
Фільтрування розчину сульфату міді
Метод2 З 3:

 Перевірте, чи можна безпечно підняти склянку над воронкою.якщо розчин ще не охолов, почекайте ще трохи до тих пір, поки зможете надійно утримувати склянку.[13]
Перевірте, чи можна безпечно підняти склянку над воронкою.якщо розчин ще не охолов, почекайте ще трохи до тих пір, поки зможете надійно утримувати склянку.[13] Струсіть розчин, обережно здійснюючи склянкою кругові рухи.після цього акуратно перелийте рідину в фільтрувальну воронку.[14]
Струсіть розчин, обережно здійснюючи склянкою кругові рухи.після цього акуратно перелийте рідину в фільтрувальну воронку.[14] Зачекайте, поки розчин просочиться крізь фільтрувальний папір.в результаті в колбі повинна виявитися прозора синя рідина. Якщо рідина буде каламутною і з чорною суспензією, повторюйте процес фільтрування до тих пір, поки вона не очиститься.[15]
Зачекайте, поки розчин просочиться крізь фільтрувальний папір.в результаті в колбі повинна виявитися прозора синя рідина. Якщо рідина буде каламутною і з чорною суспензією, повторюйте процес фільтрування до тих пір, поки вона не очиститься.[15]
Метод3 З 3:
Вирощування кристалів сульфату міді
Метод3 З 3:
 Сполосніть склянку.він знадобиться вам для вирощування кристалів. Стакан повинен бути чистим, щоб не забруднити відфільтрований розчин.
Сполосніть склянку.він знадобиться вам для вирощування кристалів. Стакан повинен бути чистим, щоб не забруднити відфільтрований розчин. Залийте прозорий синій розчин у склянку.Будьте при цьому обережні і не обпечіться, оскільки розчин може бути ще гарячим.
Залийте прозорий синій розчин у склянку.Будьте при цьому обережні і не обпечіться, оскільки розчин може бути ще гарячим. Поставте склянку в тепле місце на тиждень або довший термін.у міру випаровування води в ньому почнуть утворюватися кристали.[16]
Поставте склянку в тепле місце на тиждень або довший термін.у міру випаровування води в ньому почнуть утворюватися кристали.[16]- Процес випаровування зайвої води може розтягнутися на кілька тижнів, в залежності від того, наскільки тепло в місці зберігання склянки. Після випаровування води в склянці виростуть красиві кристали.[17]
- Можна також розігріти розчин на бунзеновской пальнику і почекати, поки випарується половина або дві третини води. Після цього дайте розчину охолонути. Цей метод, швидше за все, призведе до утворення кристалів неправильної форми.[18]
Попередження
Врахуйте, що сульфат міді є токсичним. Його не можна ковтати. Дійте обережно і завжди мийте руки після того, як торкалися до сульфату міді.
Що вам знадобиться
- Оксид міді
- сірчана кислота
- захисні окуляри
- скляний хімічний стакан
- Конічна колба
- Лопаточка
- скляна паличка для перемішування
- Чашка для випарювання
- Бунзенівський пальник
- тринога
- Фільтрувальний папір
- фільтрувальна воронка
Схожі статті
Джерела
- ↑ Http://npic.orst.edu/factsheets/cuso4gen.html
- ↑ Https://hamptonresearch.com/kids.aspx?id=4
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.nuffieldfoundation.org/practical-chemistry/reacting-copperii-oxide-sulfuric-acid
- ↑ Http://www.scienceprojectlab.com/growing-crystal.html
- ↑ Http://www.scienceprojectlab.com/growing-crystal.html