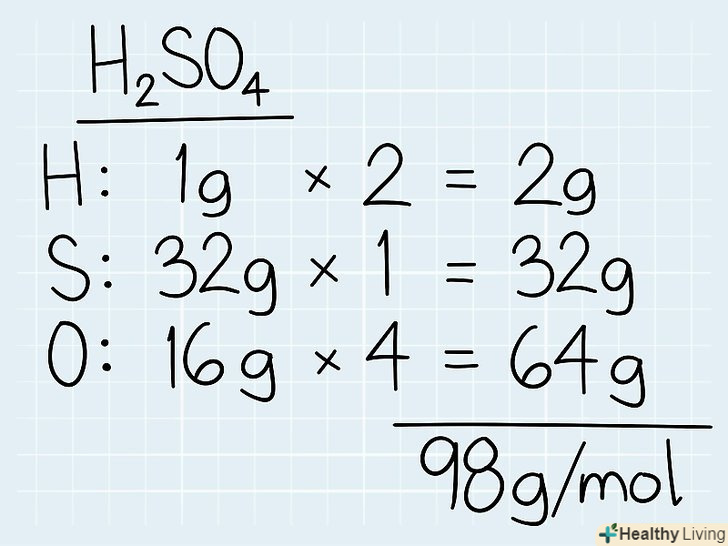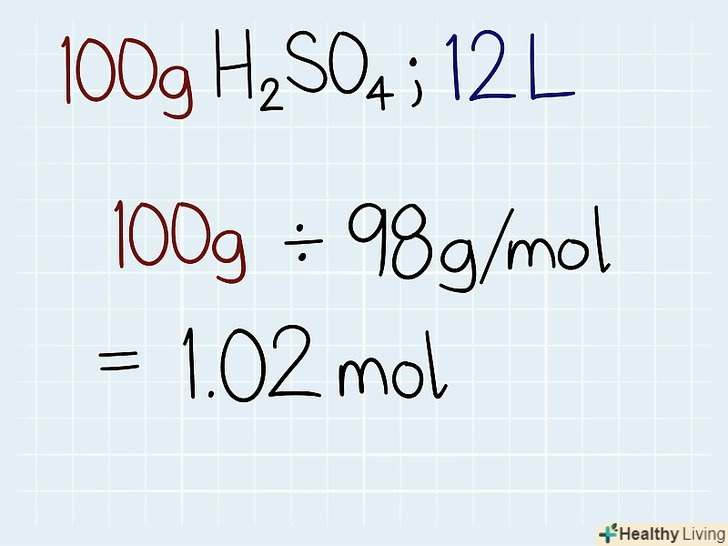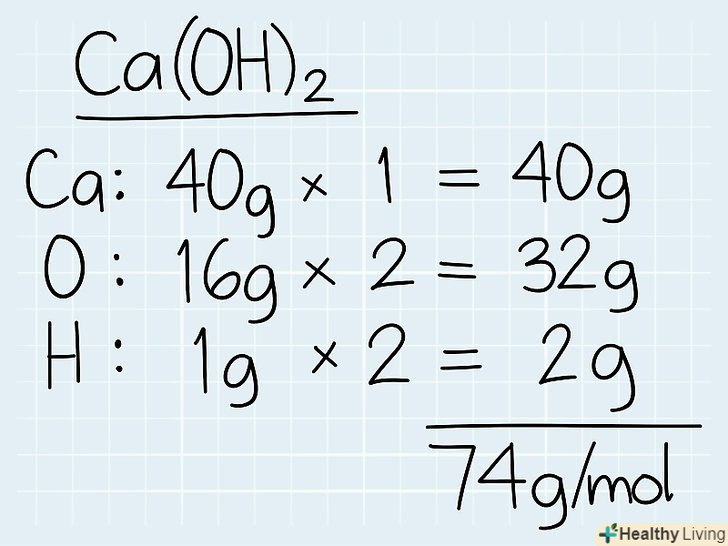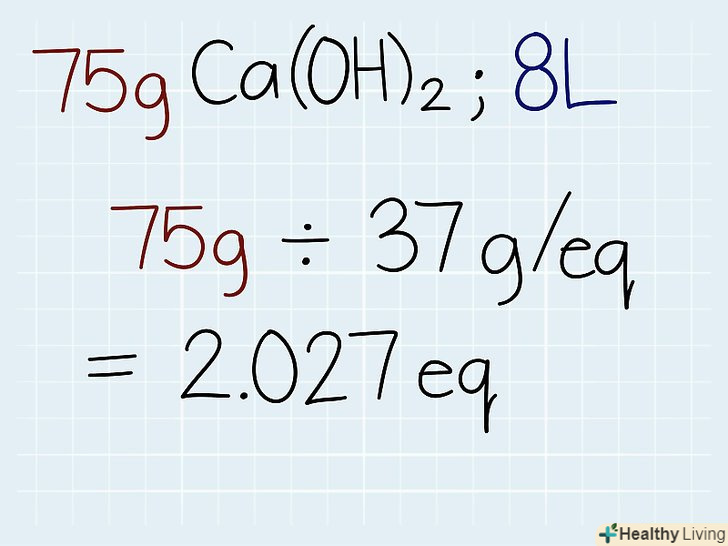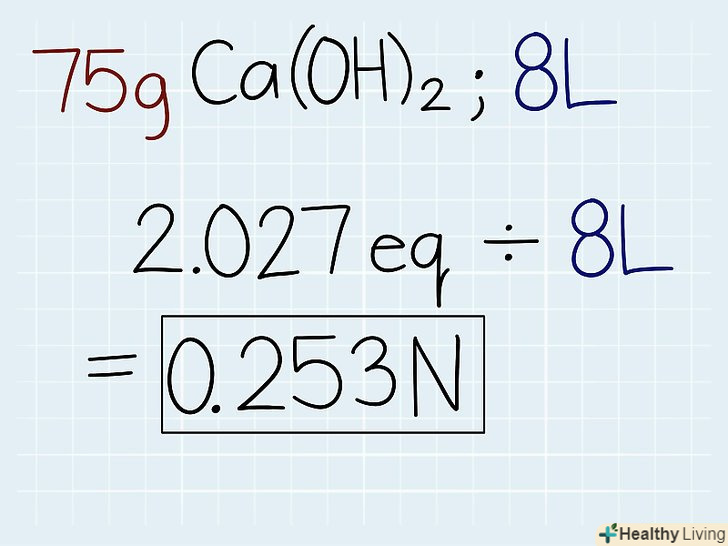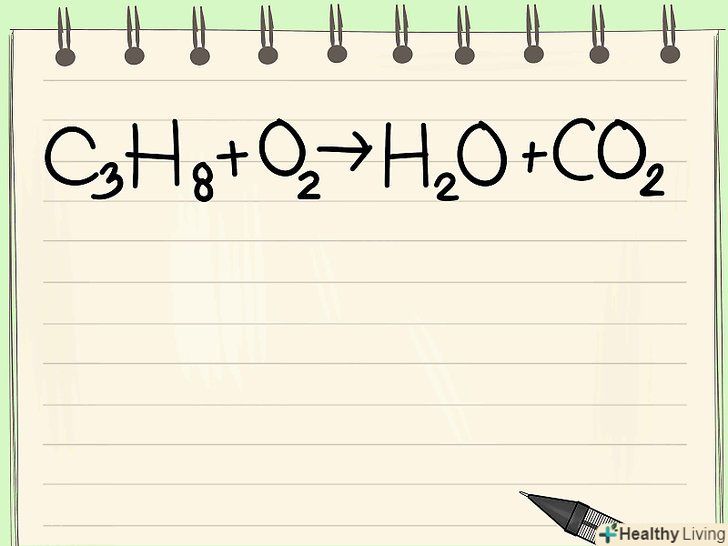Нормальність відображає концентрацію кислоти або лугу в розчині. Щоб дізнатися нормальність розчину, в розрахунках можна використовувати якмолярність, так і еквівалентну масу молекули. Якщо ви вирішили використовувати молярність, використовуйте формулу N = M( n), де M — це молярність, а n — кількість молекул водню або гідроксиду. Якщо ж Ви вирішили використовувати еквівалентну масу, використовуйте формулу N = eq ÷ V, де eq-це кількість еквівалентів, а V — обсяг розчину.
Кроки
Метод1 З 2:
Розрахунок нормальності через молярність
Метод1 З 2:
 Складіть молярну масу всіх компонентів розчину. знайдіть елементи хімічної формули на періодичній таблиці, щоб дізнатися їх атомну масу, яка відповідає молярній. Запишіть молярну масу кожного елемента і помножте її на кількість цих елементів. Складіть молярну масу всіх компонентів, щоб дізнатися загальну молярну масу.[1]
Складіть молярну масу всіх компонентів розчину. знайдіть елементи хімічної формули на періодичній таблиці, щоб дізнатися їх атомну масу, яка відповідає молярній. Запишіть молярну масу кожного елемента і помножте її на кількість цих елементів. Складіть молярну масу всіх компонентів, щоб дізнатися загальну молярну масу.[1]- Наприклад, якщо необхідно дізнатися молярну масу сірчаної кислоти (H2SO4), дізнайтеся молярну масу водню (1 г), сірки (3 г) і кисню (16 г).
- Помножте масу на кількість компонентів у складі. У нашому прикладі присутні 2 атома водню і 4 атома кисню. Загальна молярна маса водню дорівнює 2 x 1 г = 2 г. молярна маса кисню в цьому розчині буде дорівнює 4 x 16 г = 64 г.
- Складіть всі молярні маси разом. У вас вийде 2 г + 32 г + 64 г = 98 г/моль.
- Якщо ви вже знаєте молярність шуканого розчину, перейдіть відразу до кроку 4.
 Розділіть фактичну масу розчину на молярну масу. Дізнайтеся фактичну масу розчину. Вона буде вказана або на ємності з розчином, або в самій задачі. Після цього розділіть масу розчину на загальну молярну масу, знайдену раніше. Результатом стане кількість молей в розчині, після якого має бути написано «моль».[2]
Розділіть фактичну масу розчину на молярну масу. Дізнайтеся фактичну масу розчину. Вона буде вказана або на ємності з розчином, або в самій задачі. Після цього розділіть масу розчину на загальну молярну масу, знайдену раніше. Результатом стане кількість молей в розчині, після якого має бути написано «моль».[2]- Наприклад, якщо ви намагаєтеся дізнатися нормальність 100 г h2SO4, яку розчинили в 12 літрах рідини, використовуйте фактичну масу і розділіть її на молярну. В результаті у вас вийде: 100 г ÷ 98 г/моль = 1,02 моль.
- 1 моль дорівнює 6.02 x 1023 атомам або молекулам розчину.
 Розділіть результат на обсяг розчину в літрах, щоб дізнатися молярність.візьміть тільки що обчислену кількість молей в розчині і розділіть його на загальний обсяг вимірюваного розчину. В результаті ви дізнаєтеся молярність (M), за допомогою якої можна дізнатися концентрацію розчину.[3]
Розділіть результат на обсяг розчину в літрах, щоб дізнатися молярність.візьміть тільки що обчислену кількість молей в розчині і розділіть його на загальний обсяг вимірюваного розчину. В результаті ви дізнаєтеся молярність (M), за допомогою якої можна дізнатися концентрацію розчину.[3]- Виходячи з нашого прикладу, вийде така формула: 1.02 моль ÷ 12 л = 0.085 M.
Порада: обов'язково переведіть об'єм розчину в літри, якщо ще цього не зробили. В іншому випадку ви отримаєте неправильну відповідь.
 Помножте молярність на кількість молекул водню або гідроксиду.Погляньте на хімічну формулу, щоб дізнатися кількість атомів водню (H) в кислоті або молекул гідроксиду в (ОН) в основі. Потім помножте молярність розчину на кількість молекул водню або гідроксиду в цьому розчині, щоб дізнатися нормальну концентрацію, або нормальність. В кінці відповіді напишіть скорочення "N".[4]
Помножте молярність на кількість молекул водню або гідроксиду.Погляньте на хімічну формулу, щоб дізнатися кількість атомів водню (H) в кислоті або молекул гідроксиду в (ОН) в основі. Потім помножте молярність розчину на кількість молекул водню або гідроксиду в цьому розчині, щоб дізнатися нормальну концентрацію, або нормальність. В кінці відповіді напишіть скорочення "N".[4]- У нашому прикладі у сірчаної кислоти (H2SO4) 2 атома водню. Значить формула буде такою: 0,085 M x 2 = 0,17 N.
- В іншому прикладі у гідроксиду натрію (NaOH) з молярністю 2 m всього 1 молекула гідроксиду. Отже, формула буде наступною: 2 M x 1 = 2 N.
Метод2 З 2:
Розрахунок нормальності через еквівалентну масу
Метод2 З 2:
 Дізнайтеся загальну молярну масу розчину.Погляньте на хімічну формулу розчину і знайдіть кожен елемент в періодичній таблиці. Запишіть молярну масу кожного елемента і помножте її на кількість цих елементів у формулі. Складіть разом всі молярні маси, щоб дізнатися загальну молярну масу в грамах.[5]
Дізнайтеся загальну молярну масу розчину.Погляньте на хімічну формулу розчину і знайдіть кожен елемент в періодичній таблиці. Запишіть молярну масу кожного елемента і помножте її на кількість цих елементів у формулі. Складіть разом всі молярні маси, щоб дізнатися загальну молярну масу в грамах.[5]- Наприклад, якщо ви хочете дізнатися молярну масу Ca (OH)2,тоді дізнайтеся молярну масу кальцію (40 г), кисню (16 г) і водню (1 г).
- У Формулі 2 атома кисню і водню. Загальна маса кисню буде наступною: 2 x 16 г = 32 Г. молярна маса водню буде дорівнює: 2 x 1 г = 2 г.
- Складіть разом всі молярні маси, щоб отримати 40 г + 32 г + 2 г = 74 г/моль.
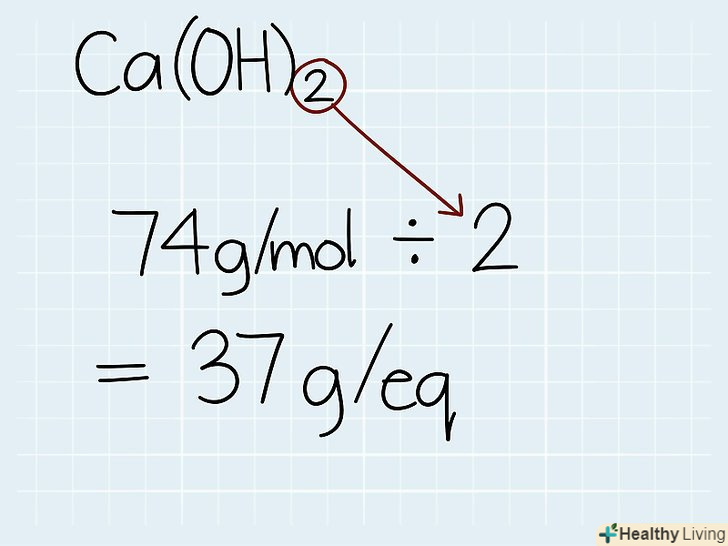
 Розділіть молярну масу на кількість молекул водню або гідроксиду.дізнайтеся кількість атомів водню (H) в кислоті або молекул гідроксиду (ОН) в основі. Розділіть щойно отриману загальну молярну масу на кількість атомів або молекул, щоб дізнатися вагу 1 еквівалента, який буде дорівнює масі 1 молі водню або гідроксиду. В кінці відповіді напишіть скорочення " Г. - Е.", що означає масу еквівалента.[6]
Розділіть молярну масу на кількість молекул водню або гідроксиду.дізнайтеся кількість атомів водню (H) в кислоті або молекул гідроксиду (ОН) в основі. Розділіть щойно отриману загальну молярну масу на кількість атомів або молекул, щоб дізнатися вагу 1 еквівалента, який буде дорівнює масі 1 молі водню або гідроксиду. В кінці відповіді напишіть скорочення " Г. - Е.", що означає масу еквівалента.[6]- У нашому прикладі у Ca (OH)2 2 дві молекули водню, значить, маса еквівалента буде дорівнює 74 г / моль ÷ 2 = 37 Г. - Е.
 Розділіть фактичну масу розчину на масу еквівалента.після того, як ви дізнаєтеся масу еквівалента, розділіть її на масу розчину, яка вказана на ємності з розчином або в розв'язуваної задачі. Відповіддю стане кількість еквівалентів в розчині, щоб ви потім змогли розрахувати нормальність. В кінці відповіді поставте скорочення»е. " [7]
Розділіть фактичну масу розчину на масу еквівалента.після того, як ви дізнаєтеся масу еквівалента, розділіть її на масу розчину, яка вказана на ємності з розчином або в розв'язуваної задачі. Відповіддю стане кількість еквівалентів в розчині, щоб ви потім змогли розрахувати нормальність. В кінці відповіді поставте скорочення»е. " [7]- Якщо в нашому прикладі 75 г Ca (OH)2, то формула буде такою: 75 г ÷ 37 Г. - Е = 2,027 е.
 Розділіть число еквівалентів на обсяг розчину в літрах.дізнайтеся загальний обсяг розчину і запишіть відповідь в літрах. Візьміть тільки що отримане кількість еквівалентів і розділіть його на обсяг розчину, щоб дізнатися нормальність. В кінці відповіді поставте скорочення "N".[8]
Розділіть число еквівалентів на обсяг розчину в літрах.дізнайтеся загальний обсяг розчину і запишіть відповідь в літрах. Візьміть тільки що отримане кількість еквівалентів і розділіть його на обсяг розчину, щоб дізнатися нормальність. В кінці відповіді поставте скорочення "N".[8]- Якщо в розчині об'ємом 8 л знаходиться 75 г Ca (OH)2, тоді розділіть кількість еквівалентів на обсяг наступним способом: 2,027 Е. ÷ 8 л = 0,253 N.
Поради
- Нормальна концентрація, або нормальність, зазвичай використовується для вимірювання кислот і основ. Якщо вам потрібно визначити концентрацію іншого розчину, для цього, як правило, вимірюють молярність.
Що вам знадобиться
- Періодична таблиця
- Калькулятор
Джерела
- ↑ Https://youtube.com/QCZMyx_557I?t=210
- ↑ Https://youtube.com/QCZMyx_557I?t=248
- ↑ Https://youtube.com/QCZMyx_557I?t=267
- ↑ Http://www.lagoonsonline.com/laboratory-articles/normality.htm
- ↑ Https://sciencing.com/calculate-equivalent-weight-6463740.html
- ↑ Http://dl.clackamas.edu/ch105/lesson6acid_base_solutions.html
- ↑ Http://www.lagoonsonline.com/laboratory-articles/normality.htm
- ↑ Http://dl.clackamas.edu/ch105/lesson6acid_base_solutions.html